lunes, 25 de enero de 2016
miércoles, 6 de enero de 2016
Biomembranas y el medio interno de la célula
Las biomembranas como barreras selectivas

Las membranas biológicas son aquellas que envuelven a toda la célula y que conforman el sistema de endomembranas con las que son delimitados compartimientos celulares. Todas las biomembranas están formadas por una bicapa fosfolipídica con aspersor aprox. 6 nm, con distintas proteínas incluidas o superpuestas (asociadas a la membrana). Además, en la cara externa de la membrana se halla un glucocáliz formado por polisacáridos. El complejo medio interno de la célula y también los orgánulos de las células eucariotas no podrían ser mantenidos de no existir las estructuras de la barrera. Ésta debe ser semipermeable (con permeabilidad selectiva) para determinados componentes, ya que la célula solo puede sobrevivir en equilibrio dinámico con su medioambiente.
Las biomembranas como barreras selectivas
- Semipermeabilidad de la membrana plasmática
La permeabilidad selectiva es una propiedad de la membrana plasmática y de otras membranas semipermeables que permiten el paso de solo ciertas partículas a través de ellas.
De esta forma, pueden entrar a la célula aquellas partículas que necesite la misma y se evita que ingresen las que no le sean útiles. De la misma forma, la célula puede eliminar las partículas que ha generado como desecho. Así se regula la entrada y salida de sustancias a través de la membrana y se logra el correcto funcionamiento de la célula.
Para que una partícula pueda atravesar la membrana plasmática debe tener un tamaño igual o menor a los poros de la membrana, debe tener la carga opuesta a la carga de la membrana o simplemente tener carga neutra, y si es más grande que los poros debe ser disuelta en una solución, disminuyendo su tamaño y así podrá entrar en la célula por medio de la membrana.
- Fenómenos de transporte en las biomembranas
La concentración de iones intracelular está regulada estrictamente. No existen solo bombas, sino también otros mecanismos de transporte en la membrana plasmática. A estos mecanismos pertenecen los canales y carrier (transportadores) que pueden regular específicamente el intercambio de iones y otras sustancias. A ellos nos hemos de referir.
Nos planteamos una "célula modelo" redonda, con membranas plasmáticas pero sin "complicaciones" como el núcleo y los orgánulos. Esta célula contiene muchos iones de K+ pero mucho menos Na+
que el medio extracelular: [K+]i
> [K+]e y [Na+]i
< [Na+]e; Esta es una situación inicial. Si una célula no tuviese mecanismo de regulación, según las leyes de la termodinámica habría difusión hasta equilibrar las concentraciones. la situación seria entonces: [K+]i
= [K+]e y [Na+]i = [Na+]e y el aspecto seria como el que muestra la figura
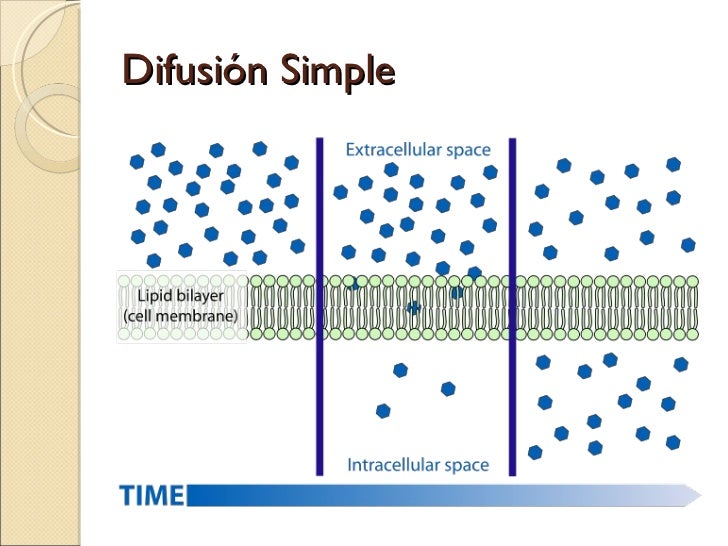
Sin
embargo, una célula viva no permite que esto ocurra. Ella transporta, Con su
bomba Na+/K+ y con consumo de ATP, el exceso de Na+ hacia
afuera y al mismo tiempo de K+ y con consumo de ATP, el exceso de Na+
hacia afuera y al mismo tiempo K+ hacia adentro.
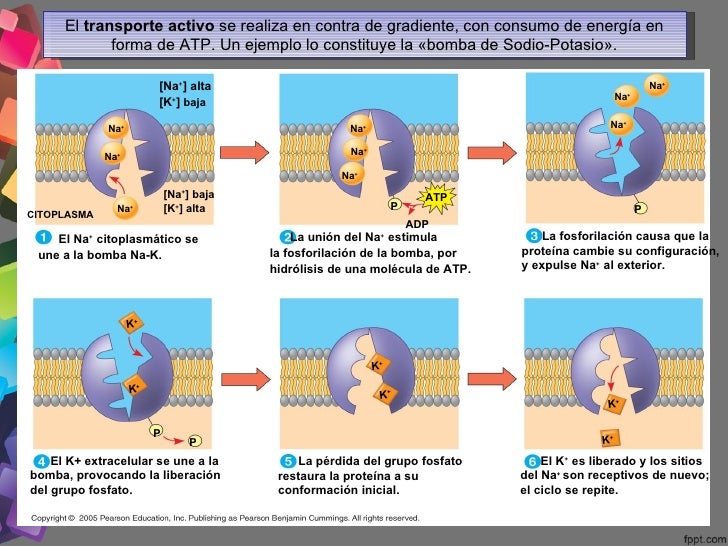
Las bombas pertenecen al transporte activo primario en el que la energía procede directamente de la escisión del trifosfato de adenosina (ATP) o de algún otro compuesto de fosfato de alta energía. Acoplan el transporte de solutos contra gradiente generando energía libre hidrolizando ATP en ADP y fosfato libre, tienen uno o más sitios para fijar el ATP en la cara citosólica de la membrana. Son muy estudiados por la farmacología ya que hay medicamentos que pueden actuar sobre estas bombas inhibiéndolas o aumentando su actividad. Se pueden distinguir cuatro tipos de bombas:
1. Tipo P
2. Tipo V (vesiculares)
3. Tipo F (mitocondriales)
4. ATPasas de la superfamilia ABC
Proteínas transportadoras
Las proteínas transportadoras determinan la permeabilidad selectiva de la membrana celular, existen 3 tipos de proteínas transportadoras dependiendo de la cantidad de sustancia que se transporta y la dirección en la que se transporta la misma.
Unitransportador, proteínas transportadoras pertenecientes al transporte pasivo o difusión, en concreto pertenecen a la difusión facilitada. Este transportador facilita la difusión de la sustancia de un lado a otro de la membrana celular. Al ser un transportador, es especifico de cada sustancia o de un grupo reducido de ellas y estas sustancias se transportan a una velocidad proporcional a la concentración de sustancia que difunde hasta alcanzar una velocidad máxima.
El mecanismo de transporte es generalmente el mismo en todos los transportadores de este tipo: Una proteína transportadora con un poro de un tamaño lo suficientemente grande como para transportar una molécula especifica a lo largo de una parte de su longitud. Esta proteína transportadora presenta un receptor de unión en el interior del transportador proteico, la molécula que se va a transportar entra en el poro y queda unida (activación química o por ligando). Después, en una fracción de segundo se produce un cambio conformacional o químico en la protína transportadora, de modo que el poro ahora se abre en el lado opuesto de la membrana. Como la fuerza de unión del receptor es débil, el movimiento térmico de la molécula unida hace que se separe y que se libere en el lado opuesto de la membrana.
La velocidad a la que se pueden transportar moléculas por este mecanismo nunca puede ser mayor que la velocidad a la que la molécula proteica transportadora puede experimentar el cambio en un sentido y en otro entre sus dos estados. Este mecanismo permite que la molécula transportada se mueva o difunda en ambas direcciones a través de la membrana.
Una característica muy importante de este tipo de transportador es que las sustancias transportadas son transportadas de una en una y siempre en una misma dirección cada vez y dado que no pertenece al transporte activo, siempre se producen las difusiones a favor de gradiente ya sea un gradiente osmótico o eléctrico en función de si lo que se transporta son sustancias como la glucosa o aminoácidos o si se trata de iones ya sean cationes o aniones.
Los transportadores más estudiados de este tipo son los que se encargan de transportar aminoácidos (la mayor parte de ellos) y glucosa.
En el caso de la glucosa se ha descubierto la molécula transportadora (GLUT), que tiene un peso molecular de aproximadamente 45.000 y que además tiene la capacidad de transportar otros monosacáridos que tienen estructuras similares a la glucosa, como es la galactosa. Sustancias como la insulina entre otras pueden actuar sobre estos transportadores modificando la velocidad de difusión, la insulina puede aumentar entre 10 y 20 veces la velocidad de difusión de la glucosa el cual es el principal mecanismo de control de la utilización de la glucosa por el cuerpo por parte de la insulina.
Cotransportador, proteínas pertenecientes al transporte activo secundario acopladas a gradientes. Por ejemplo, en una célula, debido a la bomba sodio-potasio del transporte activo primario, se transportan hacia el exterior iones sodio y se establece un gran gradiente de concentración de iones sodio a través de la membrana celular, con una concentración elevada fuera de la célula y una concentración muy baja en su interior. Este gradiente o diferencia de concentración entre los dos lados de la membrana celular representa un almacén de energía porque el exceso de sodio en el exterior de la membrana celular siempre intenta difundir hacia el interior. En condiciones adecuadas esta energía de difusión del sodio puede arrastrar otras sustancias junto con el sodio a través de la membrana celular. Para que el sodio arrastre otra sustancia con él es necesario un mecanismo de acoplamiento que se consigue por medio de otra proteína transportadora de la membrana celular. El transportador o cotransportador en este caso actúa como punto de unión tanto para el ion sodio como para la sustancia que va a ser cotransportada. El gradiente de energía del ion sodio hace que este ion y la sustancia cotransportada sean transportados juntos hacia el interior de la célula.
Las sustancias habitualmente cotransportadas mediante este sistema en las células son la glucosa y muchos aminoácidos que son transportados hacia el interior de la célula contra grandes gradientes de concentración mediante este mecanismo. La proteína transportadora tiene dos puntos de unión en su cara externa que es donde se unen las dos sustancias que van a ser transportadas hacia el interior de la célula, estos sitios de unión son uno para el sodio y otro para la glucosa o bien para un aminoácido por ejemplo. La energía suministrada para el transporte la aporta la sustancia que va a favor de gradiente y es utilizada para que la sustancia en contra de gradiente atraviese la membrana celular. Cuando ambas sustancias se unen, se produce automáticamente el cambio conformacional y ambas sustancias son transportadas al mismo tiempo. El mecanismo de cotransporte es siempre el mismo sean cuales sean las sustancias transportadas, al tratarse de proteínas transportadoras, estas son especificas de las sustancias que transportan. Los más estudiados son los transportadores de sodio-glucosa y sodio-aminoácidos, en éste último se conocen cinco proteínas transportadoras de aminoácidos, cada una de las cuales se encarga de transportar un grupo de aminoácidos con características moleculares específicas.
Este cotransporte con sodio de la glucosa y de los aminoácidos se produce especialmente a través de las células epiteliales del tubo digestivo y de los túbulos renales para favorecer la absorción de estas sustancias hacia la sangre.
Contratransporte, proteínas pertenecientes al transporte activo secundario acopladas a gradientes.
Con el mismo ejemplo que antes, los iones sodio que al estar muy concentrados en el exterior de la célula y muy poco en el interior intentan difundir hacia el interior de la célula debido a su gran gradiente de concentración. A diferencia del ejemplo anterior, la sustancia que se va a transportar junto con el sodio se encuentra en el interior de la célula y se debe transportar hacia el exterior. El ion sodio se une a la proteina transportadora en el punto en el que se proyecta hacia la superficie exterior de la membrana, mientras que la sustancia que se va a contratransportar se une a la proyección interior de la proteína transportadora. Una vez ambas sustancias se han unido a sus respectivos puntos de unión o receptores se produce un cambio conformacional y la energía que libera el ion sodio al ingresar en la célula hace que la otra sustancia se mueva hacia el exterior. Se produce un transporte en una dirección opuesta a la sustancia primaria donde la sustancia primaria que es la que se mueve a favor de gradiente de concentración o iónico es la que suministra la energía necesaria para contratransportar la sustancia secundaria que es la que se transporta en contra de su gradiente de concentración o iónico.
El contratransporte más estudiado es el que se produce con iones sodio e iones calcio e hidrógeno.
El contratransporte sodio-calcio se produce a través de todas o casi todas las membranas celulares, de modo que lo siones sodio se mueven hacia el interior y los iones calcio hacia el exterior, ambos unidos a la misma proteína transportadora en un modo de contratransporte.
El contratransporte sodio-hidrógeno se produce en varios tejidos. Un ejemplo especialmente importante se produce en los túbulos proximales de los riñones, en los que los iones sodio se desplazan desde la luz del túbulo hacia el interior de la célula tubular, mientras que los iones hidrógeno son contratransportados hacia la luz tubular. Como mecanismo para concentrar los iones hidrógeno pese a que no sea tan eficaz como el transporte activo primario de los iones hidrógeno que se produce en los túbulos renales más distales, aunque puede transportar cantidades muy grandes de iones hidrógeno, lo que hace que sea clave para el control del ion hidrógeno en los líquidos corporales.
Referencias
- http://transportedemembrana.blogspot.com.co/2011/04/bombas-del-transporte-activo.html
- Plattner. hentschel, biología celular 4 edición editorial medica panamericana
martes, 5 de enero de 2016
La sustancias que constituye a las células - componentes moleculares
Composición global de la célula
Las células eucariotas promedio está formada por agua en un 80% - 85%.La mayor parte de las sustancias sólidas consiste en proteínas, sales, polisacáridos y ácidos nucleicos.
Las sales se encuentran, sobre todo, en forma disociada como iones. la proteínas se hallan en partes disueltas y en partes como componentes estructurales o componentes de la biomembranas. Estas ultimas están compuestas principalmente pro lípidos, cuyo porcentaje en la célula global es muy variable, con dependencia de la dimensión de su sistema de endomembranas, de la presencia de abundantes plegamientos y proyecciones de la membrana plasmática y de la cantidad de lípidos que la célula almacena como material nutritivo.También la fracción correspondiente a los polisacáridos es muy variable, ya que las células almacenan cantidades muy diferentes de glúcidos. El contenido absoluto de DNA es relativamente estable, ya que cada una de nuestras células somáticas contiene la misma cantidad de material hereditario (genoma). En sus diversas formas, el RNA está vinculado con la transformación del genoma en moléculas codificadas por el DNA. Como en este sentido las células muestran actividad muy diferente, también es muy variable su contenidos de RNA.
- Fosfolípidos
Los fosfolípidos son un tipo de lípidos anfipáticos compuestos por una molécula de alcohol, a la que se unen dos ácidos grasos y un grupo fosfato. El fosfato se une mediante un enlace fosfodiéster a otro grupo de átomos, que generalmente contienen nitrógeno, como colina, serina o etanolamina y muchas veces posee una carga eléctrica. Todas las membranas plasmáticas activas de las células poseen una bicapa de fosfolípidos.
Los fosfolípidos se dividen en fosfoglicéridos (en que el alcohol es glicerol, un alcohol de cadena corta) y esfingolípidos (el alcohol es esfingosina, un alcohol de cadena larga). Los fosfolípidos más abundantes son la fosfatidiletanolamina (o cefalina), fosfatidilinositol, ácido fosfatídico, fosfatidilcolina (o lecitina) y fosfatidilserina.
Las funciones de los fosfolípidos son:
-Componente estructural de la membrana celular: El carácter anfipático de los fosfolípidos les permite su autoasociación a través de interacciones hidrofóbicas entre las porciones de ácido graso de cadena larga de moléculas adyacentes de tal forma que las cabezas polares se proyectan fuera, hacia el agua donde pueden interaccionar con las moléculas proteicas y la cola apolar se proyecta hacia el interior de la bicapa lipídica.
-Activación de enzimas: Los fosfolípidos participan como segundos mensajeros en la transmisión de señales al interior de la célula como el diacilglicerol o la fosfatidilcolina que activa a la betahidroxibutirato deshidrogenasa que es una enzima mitocondrial.
-Componentes del surfactante pulmonar: El funcionamiento normal del pulmón requiere del aporte constante de un fosfolípido poco común denominado dipalmitoílfosfatidilcolina. Este fosfolípido tensoactivo es producido por las células epiteliales del tipo II e impide la atelectasia al final de la fase de espiración de la respiración.
-Componente detergente de la bilis: Los fosfolípidos, y sobre todo la fosfatidilcolina de la bilis, solubilizan el colesterol. Una disminución en la producción de fosfolípido y de su secreción a la bilis provoca la formación de cálculos biliares de colesterol y pigmentos biliares.
-Síntesis de sustancias de señalización celular: El fosfatidinol y la fosfatidilcolina actúan como donadores de ácido araquidónico para la síntesis de prostaglandinas, tromboxanos, leucotrienos y compuestos relacionados.
- Aminoácidos y proteínas
Un aminoácido es una molécula orgánica con un grupo amino (-NH2) y un grupo carboxilo (-COOH). Los aminoácidos más frecuentes y de mayor interés son aquellos que forman parte de las proteínas. Dos aminoácidos se combinan en una reacción de condensación entre el grupo amino de uno y el carboxilo del otro, liberándose una molécula de agua y formando un enlace amida que se denomina enlace peptídico; estos dos "residuos" de aminoácido forman un dipéptido. Si se une un tercer aminoácido se forma un tripéptido y así, sucesivamente, hasta formar un polipéptido. Esta reacción tiene lugar de manera natural dentro de las células, en los ribosomas.
La unión de varios aminoácidos da lugar a cadenas llamadas péptidos o polipéptidos, que se denominan proteínas cuando la cadena polipeptídica supera una cierta longitud (entre 50 y 100 residuos aminoácidos, dependiendo de los autores) o la masa molecular total supera las 5000 uma y, especialmente, cuando tienen una estructura tridimensional estable definida.
Los aminoácidos sufren en los seres vivos tres reacciones principales que se inician cuando un aminoácido se une con el fosfato de piridoxal formando una base de Schiff o aldimina. De ahí en adelante la transformación depende de las enzimas, que tienen en común el uso del fosfato de piridoxal como coenzima. Las reacciones que se desencadenan pueden ser:
- La transaminación, que necesita la participación de un α-cetoácido,
- La descarboxilación;
- La racemización, que es la conversión de un compuesto L en D, o viceversa. Aunque en las proteínas los aminoácidos están presentes únicamente en la configuración L, en las bacterias podemos encontrar algunos D-aminoácidos formando parte de péptidos pequeños.
- Azucares
Los azúcares, sacáridos o glúcidos, son alcoholes polivalentes con un grupo aldehído terminal y rara vez con un grupo cetona. Cuyas principales funciones en los seres vivos son el prestar energía inmediata y estructural.
La glucosa y el glucógeno son las formas biológicas primarias de almacenamiento y consumo de energía; la celulosa cumple con una función estructural al formar parte de la pared de las células vegetales, mientras que la quitina es el principal constituyente del exoesqueleto de los artrópodos.
Los glúcidos pueden sufrir reacciones de esterificación, aminación, reducción, oxidación, lo cual otorga a cada una de las estructuras una propiedad específica, como puede ser de solubilidad.
Los glúcidos desempeñan diversas funciones, entre las que destacan la energética y la estructural.
- Glúcidos energéticos
Los monosacáridos y los disacáridos, como la glucosa, actúan como combustibles biológicos, aportando energía inmediata a las células; es la responsable de mantener la actividad de los músculos, la temperatura corporal, la presión arterial, el correcto funcionamiento del intestino y la actividad de las neuronas. Los glúcidos aparte de tener la función de aportar energía inmediata a las células, también proporcionan energía de reserva a las células.
- Glúcidos estructurales
Algunos polisacáridos forman estructuras esqueléticas muy resistentes -Mureína o Peptidoglicano: Componente de las paredes celulares de bacterias. -Lipopolisacáridos: Componente de la membrana externa de bacterias Gram (-). -Celulosa: Componente de la pared celular vegetal. -Quitina: Compone el exo-esqueleto de artrópodos como los insectos y crustáceos y la pared de células de hongos. -Mucopolisacáridos: Forman parte de la matriz de tejidos conectivos.
Además podemos encontrar glúcidos formando parte de la estructura de otras biomoléculas como proteínas, lípidos, y ácidos nucleicos.
Las principales rutas metabólicas de los glúcidos son:
-Glicólisis. Oxidación de la glucosa a piruvato.
-Fermentación. La glucosa se oxida a lactato (fermentación láctica), o etanol y CO2 (fermentación alcohólica).
-Gluconeogénesis. Síntesis de glucosa a partir de precursores no glucídicos.
-Glucogenogénesis. Síntesis de glucógeno.
-Ciclo de las pentosas. Síntesis de pentosas para los nucleótidos.
En el metabolismo oxidativo encontramos rutas comunes con los lípidos como son el ciclo de Krebs y la cadena respiratoria. Los oligo y polisacáridos son degradados inicialmente a monosacáridos por enzimas llamadas glicósido hidrolasas. Entonces los monosacáridos pueden entrar en las rutas catabólicas de la glucosa.
La principal hormona que controla el metabolismo de los glúcidos es la insulina.
- Bases purinas y pirimidina de los ácidos nucleicos
La purina es una base nitrogenada, un compuesto orgánico heterocíclico aromático. La estructura de la purina está compuesta por dos anillos fusionados, uno de seis átomos y el otro de cinco.
Dos de las bases de los ácidos nucleicos, adenina (también llamada 6-aminopurina) y guanina (o 2-amino-6-oxo-purina), son derivados de una purina. En el ADN (ácido desoxirribonucleico, almacenador principal y fundamental de la información genética en todos los seres vivos), estas bases se unen con sus pirimidinas complementarias, latimina (2,4-dioxi-5-metilpirimidina) y la citosina (2-oxi-4-aminopirimidina), a través de enlaces de hidrógeno.
En el ARN (ácido ribonucleico, encargado principalmente de copiar y transimitir la información genética en todos los seres vivos), la complementaria de la adenina es el uracilo (o 2,4-dioxipirimidina) en vez de la timina:
Referencia
Plattner. Hentschel. Biología celular, 4 edicion, editorial medica panamericana
Suscribirse a:
Entradas (Atom)